Jenis Baterai dan Kegunaanya
Baterai adalah sumber daya paling umum untuk perangkat genggam dasar untuk aplikasi industri skala besar. Baterai dapat didefinisikan sebagai;
kombinasi dari satu atau lebih sel elektrokimia yang mampu mengubah energi kimia yang tersimpan menjadi energi listrik.
Baterai adalah perangkat, yang terdiri dari berbagai sel volta. Setiap sel volta terdiri dari dua setengah sel yang dihubungkan secara seri oleh elektrolit yang memegang anion dan ion . Satu setengah sel termasuk elektrolit dan elektroda tempat ion bergerak, yaitu anoda atau elektroda negatif; separuh sel lainnya termasuk elektrolit dan elektroda tempat ion cat bergerak, yaitu katoda atau elektrode positif.
Dalam reaksi redoks yang menggerakkan baterai, reduksi terjadi pada kation di katoda, sementara oksidasi terjadi pada anion di anoda. Elektroda tidak saling bersentuhan tetapi terhubung secara elektrik dengan elektrolit. Sebagian besar sel setengah memiliki elektrolit yang berbeda. Semua hal yang dipertimbangkan setiap setengah sel diapit dalam wadah dan pemisah yang berpori ke ion tetapi tidak sebagian besar elektrolit mencegah pencampuran.
Setiap setengah sel memiliki gaya gerak listrik (Emf), ditentukan oleh kapasitasnya untuk mendorong arus listrik dari interior ke luar sel. Ggl net dari sel adalah perbedaan antara emf dari setengah selnya. Dengan cara ini, jika elektroda memiliki emf dan dengan kata lain, net emf adalah perbedaan antara potensi reduksi dari setengah reaksi.
Bagaimana cara merawat Baterai?
Untuk menjaga baterai dalam kondisi baik, pemerataan baterai diperlukan. Karena penuaan, semua sel tidak mengisi sama dan beberapa sel menerima muatan sangat cepat sementara yang lain mengisi secara bertahap. Penyetaraan dapat dilakukan dengan sedikit lebih dari mengisi baterai untuk memungkinkan sel-sel yang lebih lemah juga untuk mengisi penuh. Tegangan terminal dari baterai yang terisi penuh adalah 12 V, baterai mobil menunjukkan 13.8V di terminalnya sementara baterai 12 volt berbentuk tabung akan menunjukkan 14.8V. Baterai mobil harus terpasang dengan kuat di dalam kendaraan agar tidak goyang. Baterai inverter harus ditempatkan pada papan kayu jika memungkinkan.
2 Jenis Baterai
1) Baterai Primer:
Seperti namanya menunjukkan baterai ini dimaksudkan untuk penggunaan Sekali. Setelah baterai ini digunakan mereka tidak dapat diisi ulang karena perangkat tidak mudah reversibel dan bahan aktif mungkin tidak kembali ke bentuk aslinya. Produsen baterai merekomendasikan untuk mengisi ulang sel primer.
Beberapa contoh untuk baterai sekali pakai adalah AA normal, baterai AAA yang kita gunakan di jam dinding, televisi remote dll.
2) Baterai Sekunder:
Baterai sekunder juga disebut sebagai baterai yang dapat diisi ulang. Baterai ini dapat digunakan dan mengisi kembali secara bersamaan. Mereka biasanya dirakit dengan bahan aktif, aktif dalam keadaan habis. Baterai yang dapat diisi ulang diisi ulang dengan menerapkan arus listrik, yang membalikkan reaksi kimia yang terjadi selama debit. Pengisi daya adalah perangkat yang memasok arus yang diperlukan.
Beberapa contoh untuk baterai yang dapat diisi ulang ini adalah baterai yang digunakan dalam ponsel, pemutar MP3, dll. Perangkat seperti alat bantu dengar dan jam tangan menggunakan sel-sel miniatur dan di tempat-tempat seperti pertukaran telepon atau pusat data komputer, baterai yang lebih besar digunakan.
Jenis Baterai Sekunder (dapat diisi ulang):
SMF, Asam Timbal, Li dan Nicd
Baterai SMF:
SMF adalah baterai bebas perawatan yang disegel, yang dirancang untuk menawarkan daya pemeliharaan yang andal, konsisten, dan rendah untuk aplikasi UPS. Baterai ini dapat dikenakan aplikasi siklus dalam dan perawatan minimum di daerah pedesaan dan defisit daya. Baterai ini tersedia dari 12V.
Dalam dunia informatif saat ini, seseorang tidak dapat mengabaikan persyaratan untuk sistem baterai yang dirancang untuk memulihkan data dan informasi yang berkualitas penting dan menjalankan instrumentasi dasar untuk jangka waktu yang diinginkan. Baterai diperlukan untuk menghasilkan tenaga instan. Baterai yang tidak andal dan inferior dapat menyebabkan hilangnya data dan peralatan yang dapat menyebabkan kerugian finansial bagi perusahaan. Selanjutnya, segmen UPS panggilan untuk pemanfaatan sistem baterai yang handal dan terbukti.

Baterai Lithium (Li):
Kita semua menggunakannya di perangkat portabel seperti ponsel, komputer laptop, atau alat listrik. Baterai lithium telah menjadi salah satu pencapaian terbesar dalam kekuatan portabel dalam dekade terakhir; dengan penggunaan baterai lithium, kami dapat beralih dari ponsel hitam dan putih ke ponsel warna dengan fitur tambahan seperti GPS, email, dll. Ini adalah perangkat potensial dengan kepadatan energi tinggi untuk kapasitas yang lebih tinggi. Dan baterai self-discharge yang relatif rendah. Sel-sel khusus juga dapat menyediakan arus yang sangat tinggi untuk aplikasi seperti alat-alat listrik.

Baterai Nickel Cadmium (Nicd):
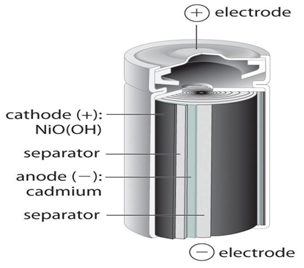
Baterai Nickel Cadmium memiliki kelebihan diisi ulang berkali-kali dan memiliki potensi yang relatif konstan selama debit dan memiliki kapasitas menahan listrik dan fisik yang lebih. Baterai ini menggunakan oksida nikel untuk katoda, senyawa kadmium untuk larutan anoda dan kalium hidroksida sebagai elektrolitnya.
Ketika baterai diisi, komposisi kimia katoda berubah dan nikel hidroksida berubah menjadi NIOOH. Di anoda, pembentukan ion Kadmium terjadi dari Cadmium Hydroxide. Ketika baterai habis, kadmium bereaksi dengan NiOOH untuk membentuk kembali hidroksida nikel dan Cadmium Hydroxide.
Cd + 2H2O + 2NiOOH -> 2Ni (OH) 2 + Cd (OH) 2
Baterai Asam Timbal:
Baterai Asam Timbal banyak digunakan dalam mobil, inverter, cadangan daya sistem dll. Tidak seperti baterai bebas tubular dan pemeliharaan, baterai Asam Timbal membutuhkan perawatan dan pemeliharaan yang tepat untuk memperpanjang umurnya. Baterai Asam Timbal terdiri dari serangkaian piring yang disimpan dalam larutan asam sulfat. Piring memiliki grid di mana bahan aktif terpasang. Piring dibagi menjadi pelat positif dan negatif. Pelat positif memegang timah murni sebagai bahan aktif sementara oksida timah melekat pada pelat negatif.
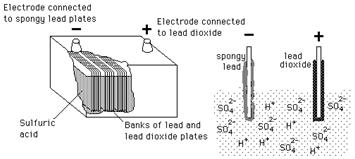
Imenghasilkan pelepasan elektron dari lempeng positif yang akan diterima oleh pelat negatif. Ini mengarah pada pembentukan potensi listrik di baterai. Elektrolit dalam baterai Asam Timbal adalah campuran asam Sulfat dan air yang memiliki berat jenis. Berat jenis adalah berat campuran asam-air dibandingkan dengan volume air yang sama. Berat jenis air bebas ion murni adalah 1.
Baterai timbal-asam memberikan nilai terbaik untuk daya dan energi per kilowatt-jam; memiliki siklus hidup terlama dan keuntungan lingkungan yang besar karena mereka didaur ulang pada tingkat yang luar biasa tinggi. Tidak ada kimia lain yang dapat menyentuh infrastruktur yang ada untuk mengumpulkan, mengangkut dan mendaur ulang baterai timbal-asam.
Seiring dengan artikel ini, baterai Lithium ion dibahas dengan kelebihan dan kekurangannya.
Bekerja dari Lithium - Ion Battery
Baterai Lithium -Ion sekarang populer di sebagian besar perangkat elektronik portabel seperti ponsel, Laptop, Kamera Digital, dll karena efisiensi daya tahan lama mereka. Ini adalah baterai isi ulang yang paling populer dengan keunggulan seperti kepadatan energi terbaik, kehilangan muatan yang dapat diabaikan dan tidak ada efek memori. Baterai Li-Ion menggunakan ion Lithium sebagai pembawa muatan yang bergerak dari elektroda negatif ke elektroda positif selama debit dan kembali saat pengisian. Saat mengisi daya, arus eksternal dari pengisi daya menerapkan tegangan berlebih dari yang ada di baterai. Hal ini akan memaksa arus mengalir ke arah sebaliknya dari elektroda positif ke negatif di mana ion-ion lithium tertanam dalam material elektroda berpori melalui proses yang disebut Interkasi. Li- ion melewati elektrolit tidak berair dan diafragma pemisah. Bahan elektroda adalah senyawa litium interkalasi.
Elektroda negatif dari baterai Li-Ion terdiri dari karbon dan elektroda positif adalah oksida logam. Bahan yang paling umum digunakan dalam elektroda negatif adalah Grafit sedangkan dalam elektroda positif mungkin Lithium kobalt oksida, Lithium ion fosfat atau Lithium mangan oksida. Garam litium dalam pelarut organik digunakan sebagai elektrolit. Elektrolit biasanya merupakan campuran karbonat organik seperti Ethylene carbonate atau Diethyl carbonate yang mengandung ion lithium. Elektrolit menggunakan garam anion seperti Lithium hexa fluoro fosfat, Lithium hexa fluoro arsenat monohidrat, Lithium per klorat, Lithium hexa fluoro borate dll. Tergantung pada garam yang digunakan, tegangan, kapasitas dan masa pakai baterai bervariasi. Litium murni bereaksi dengan air dengan kuat untuk membentuk lithium hidroksida dan ion hidrogen. Jadi elektrolit yang digunakan adalah pelarut organik tidak berair. Peran elektrokimia dari muatan elektroda antara anoda dan katoda tergantung pada arah aliran arus.
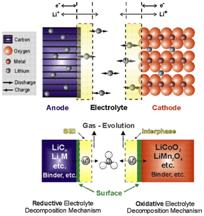
Dalam baterai Li-Ion, kedua elektroda dapat menerima dan melepaskan ion lithium. Selama proses Interkalasi, ion lithium bergerak ke elektroda. Selama proses kebalikan yang disebut de interkalasi, ion lithium bergerak kembali. Selama pemakaian, ion lithium positif akan diekstrak dari elektroda negatif dan dimasukkan ke elektroda positif. Selama proses pengisian, gerakan balik dari ion lithium terjadi.
Keuntungan dari Lithium - Ion Battery:
Baterai Lithium Ion mengungguli baterai NiCd dan baterai sekunder lainnya. Beberapa kelebihannya adalah
- Ringan dibandingkan baterai lain dengan ukuran serupa
- Tersedia dalam berbagai bentuk termasuk bentuk Datar
- Tegangan sirkuit terbuka tinggi yang meningkatkan transfer daya pada arus yang rendah
- Kurangnya efek memori.
- Tingkat debit diri sangat rendah 5-10% per bulan. Self discharge sekitar 30% dalam baterai NiCd dan NiMh.
- Baterai ramah lingkungan tanpa logam lithium gratis
Namun seiring dengan kelebihannya, seperti baterai lainnya, baterai Li-Ion juga mengalami beberapa kerugian.
Kekurangan Baterai Li-Ion:
- Endapan di dalam elektrolit dari waktu ke waktu akan menghambat aliran muatan. Hal ini meningkatkan resistansi internal baterai dan kapasitas sel untuk mengirimkan arus menurun secara bertahap.
- Pengisian tinggi dan suhu tinggi dapat menyebabkan hilangnya kapasitas
- Ketika panas, baterai Li-Ion dapat mengalami thermal run away dan ruptur sel.
- Debit yang dalam dapat menyebabkan hubungan pendek pada baterai Li-Ion. Jadi untuk mencegah hal ini, beberapa merek memiliki sirkuit mematikan internal yang mematikan baterai ketika tegangannya berada di atas tingkat aman 3 hingga 4,2 volt. Dalam hal ini, ketika baterai tidak digunakan untuk waktu yang lama, sirkuit internal akan mengkonsumsi daya dan menguras baterai di bawah tegangan yang dimatikan. Jadi untuk mengisi daya baterai seperti pengisi daya normal tidak berguna.
sumber : https://www.elprocus.com/batteries-types-working/










Leave a Comment